Что не так с российской вакциной от коронавируса? Почему на Западе ее восприняли со скепсисом?
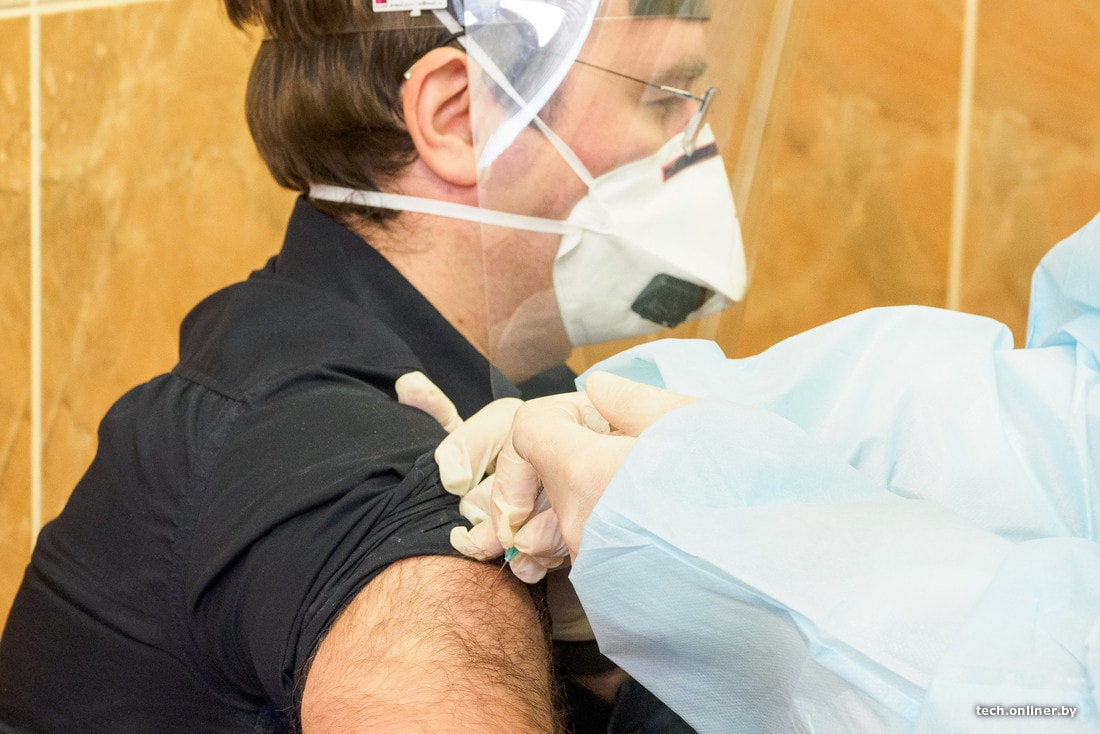
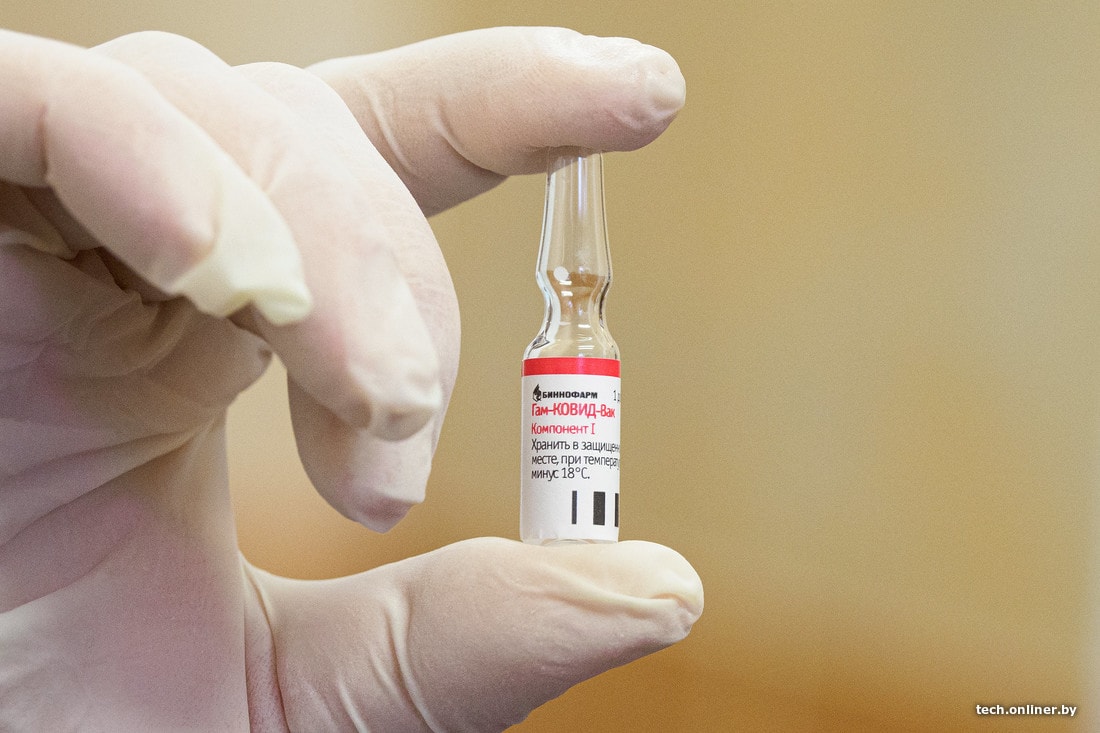
На прошлой неделе первым добровольцам в Беларуси вкололи вакцину от коронавируса «Спутник V», разработанную в Национальном центре эпидемиологии и микробиологии имени Гамалеи. В августе о регистрации первой в мире вакцины от коронавируса сообщил лично президент РФ Владимир Путин. Ее подготовили и запустили в производство в максимально короткие сроки. Но на Западе этим не впечатлились. Завидуют? Что не так с российской вакциной от коронавируса?
Замминистра здравоохранения Александр Тарасенко в понедельник отрапортовал, что первые белорусские добровольцы, на которых испытывают российскую вакцину, чувствуют себя хорошо. Всего их будет сотня человек: часть будет привита вакциной, другой части вколют плацебо. Однако подопытные до конца исследования не будут знать о том, что именно им вкололи, как и медики. В этом заключается суть непредвзятого исследования эффективности вакцины.
У западных специалистов возникли претензии именно к этапам исследования российской вакцины «Спутник V»: уж слишком быстро она получила одобрение и государственную регистрацию, минуя самый долгий и масштабный третий этап испытаний. Он включает в себя изучение вакцины, ее эффективности и, самое главное, проверку безопасности на десятках тысяч добровольцев. Надо удостовериться, что от вакцины не возникают побочные эффекты, а если какие-то осложнения и существуют, то стоит выяснить частоту их возникновения. Однако в отношении российской вакцины пока этот этап реализован не был.
Два этапа испытаний
В начале сентября в авторитетном научном журнале The Lancet была опубликована статья группы российских ученых, которые проводили первый и второй этапы тестирования вакцины. Она состоит из двух компонентов: вектора рекомбинантного аденовируса типа 26 (rAd26) и вектора рекомбинантного аденовируса типа 5 (rAd5). Оба содержат в себе гены SARS-CoV-2.
Исследования проводились этим летом, в них приняли участие 76 здоровых людей в возрасте 18—60 лет. Среди наиболее частых побочных эффектов упоминались боль в месте инъекции (у 58% привитых), гипертермия (50%), головная боль (42%), слабость (28%), мышечные и суставные боли (24%). Большинство этих явлений были умеренными. У всех участников выработались антитела к гликопротеину SARS-CoV-2. «Вакцина имеет хороший профиль безопасности и вызвала сильные гуморальные и клеточные иммунные ответы у участников. Необходимы дальнейшие исследования эффективности этой вакцины для предотвращения COVID-19», — заключают исследователи.
И если для министерства здравоохранения России эти результаты оказались достаточными, то американскому и европейскому медицинским регуляторам данных об иммунном ответе для одобрения вакцины будет недостаточно.
«Иммунный ответ не может быть прямо пропорционален степени защиты. Выяснить это можно только в крупномасштабных испытаниях», — считает Питер Опеншоу, профессор экспериментальной медицины в Имперском колледже Лондона.
Такую же мысль высказывал и Владимир Путин. Российским журналистам он рассказывал, что одна из его дочерей была привита вакциной.
«Чувствует себя хорошо, концентрация антител высокая, — сказал Путин. — Главное — обеспечить безусловную безопасность и эффективность этой вакцины в будущем».
«Когда люди начинают обходить стандартный процесс разработки вакцины, это действительно беспокоит», — предостерегает Ашиш Джа, декан факультета общественного здравоохранения Университета Брауна (США).
Открытое письмо с сомнениями
Следом за публикацией итогов исследования в The Lancet появилось открытое письмо зарубежных ученых под названием «Безопасность и эффективность российской вакцины против COVID-19: требуется дополнительная информация». Они назвали работу коллег потенциально значимой, но высказали несколько замечаний. Их смутило подозрительное совпадение количественных данных по разным испытуемым. Например, в одном из экспериментов в группе из девяти волонтеров уровень антител полностью совпадал у всех испытуемых с 21-го по 28-й день. Статистические аномалии обнаружились и в других результатах исследований.
Тем самым авторы открытого письма (а это профессора и доктора из университетов США, Италии, Австралии, Японии, Швейцарии, Германии, Франции и других стран) выразили сомнение в надежности данных, которые предоставили в своей статье их российские коллеги. Они попросили опубликовать исходные данные, использованные для построения графиков.
На это из НИЦЭМ имени Гамалеи ответили, что категорически отвергают все обвинения в недостоверности статистических данных.
«Опубликованные данные являются достоверными и точными и прошли экспертизу у пяти рецензентов The Lancet, полноразмерный клинический протокол предоставлялся в редакцию журнала. Мы представили именно те данные, которые получили, а не те, которые должны нравиться итальянским экспертам», — написал автор изначальной научной работы по вакцине Денис Логунов из НИЦЭМ.
Что касается статистической аномалии с совпадением индикаторов антител у девяти пациентов в период с 21-го по 28-й день, то Логунов объяснил это немногочисленностью группы испытуемых: «Не исключено, что показатели иммунной системы могут достичь того уровня плато, который мы наблюдали во время исследования».
Он подчеркнул, что все полученные во время исследования результаты были перепроверены дважды.
Какие еще претензии?
Помимо статистических неувязок, специалисты имеют вопросы и по небольшому количеству участников на первой и второй фазах исследований. По 38 человек в каждой фазе испытаний российской вакцины кажутся им недостаточными.
Для сравнения: в испытаниях вакцины от коронавируса, разработанной компанией AstraZeneca, которые проводятся Оксфордским университетом, на первых двух этапах принимают участие 1077 человек. В проведении второй фазы испытаний вакцины от компании Moderna участвуют около 600 человек. Вакцина, которую разработал Институт биотехнологий Академии военных медицинских наук Китая, была предоставлена пяти сотням волонтеров. То есть уже на ранних этапах привлекается достаточно внушительное число участников, тогда как в испытаниях российского «Спутника V» их было в разы меньше.
К тому же из российской научной работы не совсем понятно, был ли выдержан временной интервал между двумя фазами испытаний. Кроме того, результаты исследования опубликовали, не дожидаясь истечения 180-дневного срока после окончания наблюдений за пациентами.
В ответ на все это тот же ведущий автор исследования Денис Логунов заявил, что на самом деле, согласно протоколу исследования, пациентам назначено еще одно посещение — через 180 дней после вакцинации.
«Полученные на тот момент данные будут опубликованы в установленном порядке», — пообещал он.
В конце сентября Энрико Буччи, профессор биологии американского Университета Темпл и один из авторов открытого письма, дал возмущенный комментарий BBC. По его словам, авторы исследования российской вакцины так и не предоставили никаких данных, которые развеяли бы сомнения относительно статистических аномалий.
Пускай непрозрачность действий коллег вызывает на Западе вопросы, но в самой России считают, что предоставлять полный доступ к данным своего исследования они и не обязаны.
Елена Смолярчук, глава Центра клинического изучения лекарственных средств Сеченовского университета и руководитель первой фазы исследований «Спутника V», заявляла, что данные испытаний собираются предоставлять только заинтересованным в вакцине партнерам, а не любителям искать «компроматы, которых нет».
Такие искатели из BBC, кстати, удивились тому, как быстро пять рецензентов прочитали и одобрили научную работу россиян. Обычно самый быстрый срок рецензирования в The Lancet составляет не менее 20 рабочих дней. Однако в случае с российской статьей они справились за три недели. Журналисты попытались узнать в The Lancet всю хронологию подготовки статьи к публикации, но там делиться такой информацией отказались.
Как бы то ни было, вакцина уже одобрена. Заявляется, что ее будут миллионными тиражами поставлять в различные страны, в том числе в Беларусь. Но самое важное и полномасштабное исследование еще не проведено. Только в середине сентября стало известно, что набрано достаточное количество участников для проведения третьей фазы испытаний. Правда, этот этап называют не «третьей фазой», а «послерегистрационным исследованием».
«Всего за две недели в Москве уже набрано 55 тыс. волонтеров», — заявил Кирилл Дмитриев, глава Российского фонда прямых инвестиций (именно этот государственный фонд занимается распространением вакцины).
Пока же ни одна вакцина в мире не прошла всех клинических испытаний. Ожидается, что массовая вакцинация россиян отечественной разработкой начнется в 2021 году. Ее клинические испытания, помимо Беларуси, вскоре начнутся и в Венесуэле, где планируется привлечь 2 тыс. добровольцев.
Читайте также:
- В аэропорту Шанхая почти столкнулись два Airbus. Ошибка диспетчера могла убить 439 человек
- Откуда в Беларуси всплеск смертности во II квартале? Сравнили с другими странами
Наш канал в Telegram. Присоединяйтесь!
Есть о чем рассказать? Пишите в наш Telegram-бот. Это анонимно и быстро
Перепечатка текста и фотографий Onliner без разрешения редакции запрещена. nak@onliner.by